Index
3. Toxicité et Impacts sanitaires
4. Dispositions réglementaires
5. Résultats
6. Conclusions
7. Pour en savoir plus - sites consultables
Les CFC appartiennent à la catégorie des haloalcanes.
Les haloalcanes sont des alcanes dont un ou plusieurs atomes d’hydrogène sont remplacés par des atomes d’halogènes: F: fluor, Cl: chlore, Br: brome, I: iode).
Ils comprennent plusieurs familles dont les principales sont :
|
|
|
Schéma d’une molécule (tiré de Wikipédia) |
- les CFC: chlorofluorocarbures (les halogènes sont le fluor et le chlore), les CFC sont commercialement appelés Fréon.
- les HCFC: hydrochlorofluorocarbures (les halogènes sont le fluor et le chlore), les halons sont des composés chloro-bromé par exemple le CF2BrCl, CF3Br et le C2F4Br2.
- les HFC: hydrofluorocarbures (l’halogène est le fluor).
Il sera par la suite essentiellement question des CFC
La Nomenclature des CFC est la suivante: CFC – ABCDE, avec:
- A: nombre de doubles liaisons, omis si égal à O,
- B nombre d’atome de carbone -1,
- C nombre d’atome d’hydrogène +1,
- D nombre d’atome de fluor,
- E si isomères: a, b …
Cette nomenclature n’est pas simple ni logique. Par exemple CFC – 12 (ou Fréon 12) correspod à la formule chimique: CF2Cl2 soit celle du dichlorodifluorométhane.
Les CFC ont été synthétisés dans les années 1930.
Les haloalcanes sont des substances gazeuses à température ambiante et à pression normale. Ils sont stables, incolores, ininflammables, ils sont facilement liquéfiables par pression, non toxiques et peu coûteux.
Ils sont facilement liquéfiables par simple pression.
Ces propriétés ont permis leurs utilisations dans de nombreux secteurs industriels: 
- industries du froid: réfrigérateurs, congélateurs, climatiseurs intérieurs et de voitures etc. du fait de leur facilité de liquéfaction et leur grande vitesse d’évaporation, en particulier les fréons 11 (dichloromonofluorométhane) et 12 (dichlorodifluorométhane),

- industrie des propulseurs (laques…) du fait de leur stabilité, inertie, ininflammabilité et vitesse d’évaporation élevée,
- des nettoyants industriels car les CFC ont une grande aptitude à dissoudre les graisses,
 de l’industrie des mousses isolantes,
de l’industrie des mousses isolantes,
- de l’industrie de lutte contre les incendies (halons)
3. Toxicité et impacts sanitaires
3.1. Toxicité
La toxicité des halocarbures est quasi nulle (Voir la fiche DD/pollution de l’air/ozone).
3.2. Impacts sanitaires à long terme
Les CFC et HCFC détruisent l’ozone stratosphérique.
Ces substances se décomposent dans la haute atmosphère en gaz chlore dont chaque molécule peut détruire jusqu’à 100000 molécules d’ozone.
De plus ces gaz font partie des 6 principaux gaz à effet de serre (gaz qui interceptent les rayonnements infrarouges émis par la terre) mentionnés dans le protocole de Kyoto. Des experts estiment qu’ils étaient responsables de 10 à 25 % de l’effet de serre global.
En effet les CFC et HCFC ont une durée de vie dans l’atmosphère qui varie de plusieurs siècles jusqu’à 50 000 ans.
Leur PRG relatif à CO2 à 100 ans (100 ans correspond à la durée moyenne de «vie» du CO2 dans l’atmosphère) est de quelques centaines à plusieurs milliers.
Définition du PRG:Pouvoir de Réchauffement Global:
Le PRG d’un gaz est le rapport entre l’énergie renvoyée vers le sol en 100 ans pour 1 Kg de ce gaz et celle que renverrait 1 Kg de CO2. Le PRG dépend des concentrations et des durées de vie des gaz. Par exemple 1 Kg de méthane (CH4) et 25 Kg de CO2 émis au même moment, auront autant réchauffé l’atmosphère au bout d’un siècle.
De même un kg d’halocarbures émis dans l’atmosphère aujourd’hui produira dans un siècle le même effet que quelques centaines à quelques dizaines de milliers de kg de CO2.
Ces deux phénomènes (destruction de l’ozone stratosphérique et effet de serre) sont de nature très différente.
NB:Les HFC (hydrofluorocarbures) ne comportant pas d’atome de chlore ne détruisent pas la couche d’ozone mais sont des gaz à effet de serre. Ils sont responsables de 0,5 à 1 % de l’effet de serre global.
On observe donc que la suppression des émissions de CFC et HCFC représente un effet d’optimisation de l’effet de serre supérieur à celui du protocole de Kyoto.
Cependant les CFC montent lentement dans l’atmosphère en 15 ans environ c’est pourquoi en 2008 les CFC présents dans la stratosphère ont été produits avant 1993 alors que les CFC émis après 1993 sont en chemin pour atteindre la stratosphère.
3.3. La «couche d’ozone»ou ozonosphère
Il s’agit d’air rarifié situé dans la stratosphère à une altitude comprise entre 20 et 50 kilomètres d’altitude et enrichi en ozone (O3) à une concentration de 1 pour 100000 environ (soit 10 ppm), produit par l’action du rayonnement solaire sur le gaz oxygène (réaction de photolyse):
O2 + UV —> O + O, puis O + O2 —> O3
Cette formation d’ozone est en équilibre dynamique avec sa destruction par le rayonnement UV solaire:
O3 + UV > O2 + O (UV= rayonnement ultra violet vers 210-290 nm, soit 0,21 à 0,29 μm).
Cette réaction de destruction d’ozone permet d’arrêter les UV nocifs, ce qui protège la vie sur terre.
Les scientifiques estiment que cette «couche d’ozone» s’est formée depuis 2 milliards d’années, à partir de la formation d’oxygène sur terre. Elle a permis l’apparition et le maintien de la vie terrestre.
Cet «couche d’ozone» nous protège des rayons UV (ultraviolets), émis par le soleil, en particulier des UV-B qui sont des agents mutagènes qui détruisent l’ADN des cellules, ce qui peut engendrer des cancers, un affaiblissement du système immunitaire, des affections oculaires dont la cataracte, ralentit la photosynthèse et donc les rendements agricoles.
4. Dispositions réglementaires
 Protocole de Montréal(1987):
Protocole de Montréal(1987):
Cet accord inter gouvernemental concerne la production et l’émission des halocarbures dans l’objectif de protéger la «couche d’ozone» stratosphérique mais ne concerne pas les gaz à effet de serre en général ni la diminution des émissions d’ozone près du sol qui relève d’autres phénomènes (automobiles … voir la fiche de PFO: Développement durable et nous / le DD et l’effet de serre datée du 24 mars 2005).
La production des CFC et halons a été interdite par des accords gouvernementaux de Montréal (1987) puis révisé à Londres (1990), à Copenhague (1992), à Vienne (1995) et à Pékin et sont remplacés par d’autres gaz dont les HCFC (hydrochlorofluorocarbures) et HFC (hydrofluorocarbures), le propane et le butane, l’ammoniac qui ont une contribution plus faible pour la destruction de la couche d’ozone.
En ce qui concerne les HCFC (remplaçant les CFC) l’arrêt de la production et de l’utilisation de certaines molécules a été réalisé en 2004, leur élimination totale étant prévue entre 2030 et 2040.
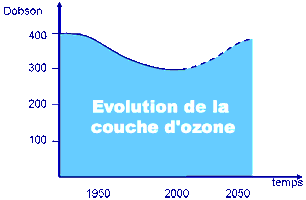
Mesures de la «couche d’ozone (unité Dobson):
 1 unité Dobson correspond à une couche d’ozone qui aurait 10 μm d’épaisseur dans des conditions normales de température et de pression.
1 unité Dobson correspond à une couche d’ozone qui aurait 10 μm d’épaisseur dans des conditions normales de température et de pression.
La «couche d’ozone «normale» a été évaluée à 400 unités Dobson soit une épaisseur normale de 4 mm d’ozone stratosphérique.
Actuellement elle a environ 300 unités Dobson.
Résultat:
Les délégués réunis à Montréal (20 ans après) le 12 septembre 2007 ont salué la réussite de l’accord de Montréal de 1987 et déclarent que la couche d’ozone retrouvera son état de 1980 vers les années 2055 à 2065.
Un grave risque sanitaire, résultant de la diminution de la «couche d’ozone» stratosphérique, a été évité grâce à la découverte de nouvelles molécules moins toxiques.
Cependant il faudra quelques décennies pour revenir à un état proche de celui des années 1950 du fait de la lente évolution de la composition atmosphérique et des contraintes lourdes, en particulier pour les pays en développement.
Certains experts estiment que cette action représente annuellement l’équivalent d’une réduction de 3 % des émissions mondiales des gaz à effet de serre –toutes choses étant égales par ailleurs- (bien que cela n’ait pas été l’objectif initial de ces accords internationaux.
7. Pour en savoir plus – sites consultables
- http://www.actu-environnement.com
- http://www.ecologie.gouv.fr
- http://www.manicore.com
- http://www.wikipedia.org






